SPECT定量的决心
随着核医学技术的不断发展,核医学影像设备也在日新月异快速进步。从1958年Anger 发明第一台开创了核医学显像新纪元的γ照相机,到20世纪80年代横空出世的初代SPECT、 PET,再到现如今不断更新迭代、集各种时代前沿科技于一身的SPECT/CT、PET/CT、以及PET/MR,核医学成像技术早已从功能学检查、定位、定性阶段过渡到了定量阶段。核医学130多年的发展历程,如今正在加速迈进精准医疗时代。
我们知道,PET/CT和SPECT/CT是核医学最重要的组成部分,它们可以无创的反映组织生理、病理和功能代谢的变化,因此广泛应用于临床疾病的诊断和分期等等。与PET相比,SPECT在某些方面已表现出了PET/CT不可比拟的优势。许多SPECT所使用的放射性核素的物理半衰期比PET的放射性核素更长,其半衰期与体内感兴趣区的生理过程更为一致。同时SPECT所使用的放射性核素更易于获取,无需医用回旋加速器,也不需要设置快速的配送网络。在一次显像过程中,SPECT可以通过使用多种不同放射性核素标记的示踪剂,对多种不同的生物过程进行显像[1]。除此之外,SPECT/CT还能开展核素治疗,实现诊疗一体化[2]。相比于PET/CT,SPECT/CT价格经济,使用范围更广更便捷。并且,SPECT检查也已纳入我国医保,可以惠及更多患者的临床检查。
因此,在我们迈向精准医疗的过程中,可靠而准确的SPECT定量成像显得尤为宝贵。
SPECT定量的困局
然而SPECT定量之路并非一帆风顺。与SPECT相比,为人熟知的PET检查之所以能被临床医师、学术界以及广大患者充分认可,究其原因是与PET对病灶SUV的定量密不可分。通过PET/CT得到的精准SUV定量值能够量化反映放射性核素在体内的分布情况,为临床诊断、分期、治疗方案选择、随访和疗效评估提供了更有利的指导和更重要的临床意义,这也就是传统实体瘤疗效评估的RECIST标准已经发展为PERCIST标准的理论依据。
但是,传统SPECT则被认为是非定量化的成像方式。PET/CT数据重建的体素值是以单位体积的放射性活度(Bq/ml)为单位,无需单位转换即可获得定量SUV值,其定量的准确性得到临床的广泛认可,而SPECT探测单光子的工作原理与PET的双光子符合探测方法不同,建出的图像是以计数(Counts/Voxel)为基础,因此加大了SPECT定量测量的难度。
此外,最常见的SPECT的重建算法是OSEM,这一算法在低计数率的情况下适应性有限(SPECT的灵敏度比PET低1-2个数量级),且缺少灵敏度校准的标准工具;由成像原理所决定,SPECT的衰减校正比PET难度更高,早期的SPECT大多不带衰减校正,SPECT/CT出现以后才逐渐变得普及;SPECT涉及的γ光子能量因放射性核素不同而不同,加之不同种类准直器的使用,使得情况较PET更为错综复杂。JNM的文章也曾指出“PET的灵敏度和空间分辨率都优于SPECT,同时PET可以实现组织内的精准定量”[3],换言之,SPCET真的很难实现定量或精准定量。
当然,科学家对于SPECT的SUV定量的探索从未停止。在搜索引擎输入“SPECT、SUV、定量”,你会得到上千个相关结果:国内外诸多临床和科研机构都能通过软件单位转换的办法求得SUV值,并有发表相关文章。但,单纯依赖软件转换,是难以实现SPECT精确定量,更无法有效的进行疗效评估。
传统SPECT定量技术:软件单位转换
传统SPECT定量是以计数(Counts/Voxel)为基本单位,在SPECT图像完成采集、重建之后,利用自制的放射性容器(注射器)测得的转换因子来计算Bq/mL,最后带入公式求得SUV值。这样低成本且技术路线简单的方法看似可以应用于所有SPECT定量,然而实际上却无法实现本质上的定量[4-5],且临床应用也是极少。那它究竟有什么样的致命缺陷呢?
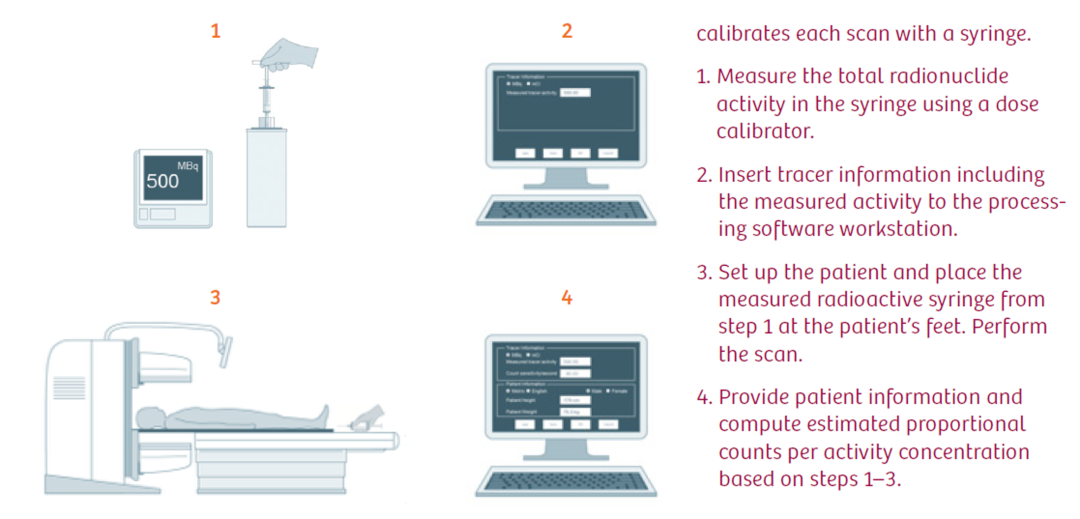
传统SPECT定量(软件单位转换)流程图

首先,单位转换发生于图像采集、重建完成之后,图像本质上来源于非定量系统,未能克服传统SPECT/CT固有的定量障碍(系统灵敏度校正、采集时探头运动位差、准直器自身特性校正及与相应核素的匹配、探头采集时与目标距离、空间分辨率、衰减校正、散射校正、衰变校正等因素均会严重影响定量的准确性)[1],图像无法满足精确定量需求。
其次,软件单位转换定量技术中,转换因子和死时间校正必须现用现测,只对同一设备的固定时间点有效,无法实现不同设备、不同时间之间定量的可重复性。
再者,每次均需延长或增加采集范围,加上注射器内的药物放射性,将显著增加患者辐射剂量。
Bailey等长期致力于定量SPECT的研究,他们认为厂商需要在SPECT系统中就开始提供校准技术,明确定量SPECT的操作限制,并将其列入常规SPECT质量控制程序中。精准的SPECT定量需要同时对系统的硬件和软件进行改进。SPECT定量除了传统方法提供的校正方法外,需要考虑以下因素:
1. 系统运动导致的性能漂移;
2. 系统灵敏度的测量;
3. 不同的放射性核素、闪烁晶体厚度、准直器及脉冲高度分析器能窗的使用导致的差异;
4. 明确散射校正的算法参数,使用不同的放射性核素和准直器时,各参数也各不相同。
因此,建立便于临床操作、精准、可重复的定量SPECT平台面临大量的技术挑战,却也迫在眉睫[6]。
Broad Quantification
——“精准定量SPECT/CT系统” 时代的到来
终于,直到2013年,西门子经过多年研究,首款Symbia Intevo系列的SPECT/CT问世。它实现了从硬件到软件的SUV值精准定量设计,为核医学行业带来了革命性的进步。
为了排除系统硬件设备对定量结果的影响,Intevo推出清云探头和三维自适应机架减少采集过程中的空间位差;独有的准直器虹膜技术实测准直器小孔的光学性能;高清弱源3D识别技术真实反映探头在不同位置和角度对点源的响应;自适应双线性CT衰减校正;基于原始投影的衰变校正;OSCG共轭梯度重建技术等等。
除此之外,随着治疗核素的广泛应用,如何实现全核素治疗的精准定量,进而实现SPECT/CT诊疗一体化的精准量化评估,也成为了业界面临的重点问题。西门子面对临床难题,对核心技术开拓创新,推出了全新一代精准定量2.0平台——Broad Quantification。该定量平台的SUV值源于采集与重建,直接以绝对放射性活度构建图像(与PET相似),其图像原始单位即为Bq/mL,无需软件转换,可在其他工作站中进行定量分析。
Broad Quantification还可以实现全核素精准定量,并将全核素定量误差范围控制在10% 以内,此项数据不仅获得中国药监局NMPA及美国FDA的双重认证,也是唯一获得美国FDA认证的SPECT全核素精准定量方式。
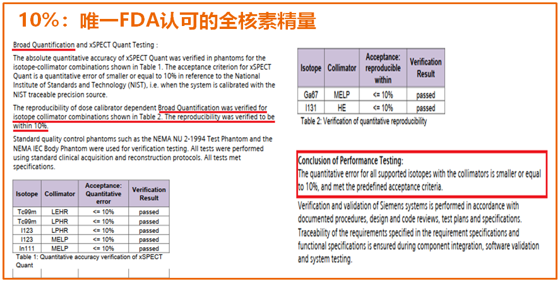
基于以上先进技术,西门子Symbia Intevo SPECT/CT结合搭载的定量平台不仅能实现不同患者、不同时间、不同系统之间的精准、可重复的定量,并且其定量操作流程与常规SPECT扫描并无区别,具有高度的临床实用性。医学权威期刊JNM和EJNMMI的两篇综述性文章也指出:SPECT的潜力(即定量化分析)值得期待,精准定量SPECT为临床服务的新时代已经到来!值得一提的是,作者将Intevo SPECT/CT精准定量的诞生评价为“特别鼓舞人心(particularly encouraging)”。

目前,关于Symbia Intevo精准定量的专利和科研文章不胜枚举,越来越多的临床医师享受到了SPECT的SUV值为科研和临床应用开启的一片广阔天地。
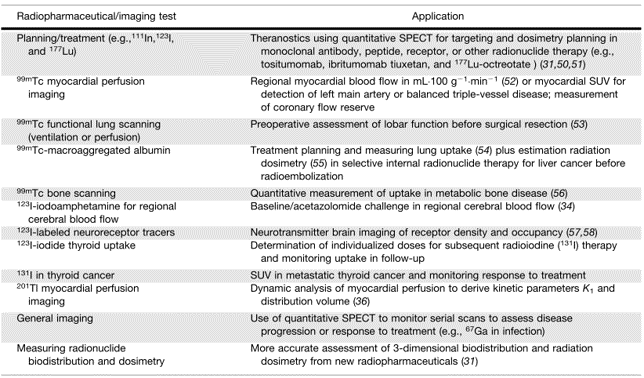
定量SPECT/CT潜在临床科研应用
精准定量SPECT,The Time is NOW
西门子Symbia Intevo精准定量SPECT/CT系统,从硬件到软件专为定量量身定制,是真正且独一无二做到精确且可重复测量的SUV定量工具,为临床工作、科学研究以及学科发展提供了强有力的武器。今时今日,此时此刻,精准定量SPECT/CT系统已然来到,让我们向着更深、更新的领域迈进,去探索期待已久的未至之境。